Compuestos químicos curiosos: el tiofeno y el selenofeno
Escrito por Quimitube el 22 mayo
Probablemente la mayoría de personas que hayan tenido un acercamiento a la química a nivel de bachillerato o de primer curso universitario habrá visto alguna vez este compuesto orgánico heterocíclico con oxígeno, el furano:
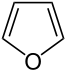
El furano es un líquido incoloro (aunque a veces puede tomar un color marronoso por la presencia de impurezas) altamente inflamable y muy tóxico, tanto para la salud humana como para el medio ambiente. Su punto de ebullición es de 31,3ºC, es decir, próximo a la temperatura ambiente, lo que hace que tenga que guardarse refrigerado para evitar que se inflame de forma espontánea. Se trata, además, de un compuesto aromático, lo que lo hace especialmente estable. ¿Por qué es aromático? Aunque a veces se asocia la aromaticidad únicamente a aquellos compuestos que poseen anillos bencénicos, es decir, ciclos de seis con tres enlaces dobles alternados, la presencia de dobles enlaces conjugados (en carbonos alternativos) y de un átomo con pares electrónicos libres como el oxígeno hace que dichos electrones puedan circular con cierta libertad, y eso es lo que estabiliza la molécula; en el furano ocurre esto, el ciclo presenta dos dobles enlaces conjugados y un heteroátomo con un par electrónico «disponible», por lo que es un compuesto bastante estabilidad. En la imagen siguiente se puede observar la distribución de la densidad electrónica por encima y por debajo del plano en el furano, comparada con la del benceno:
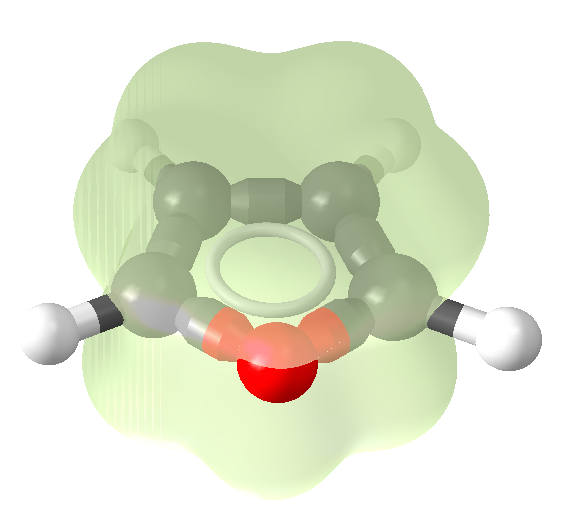
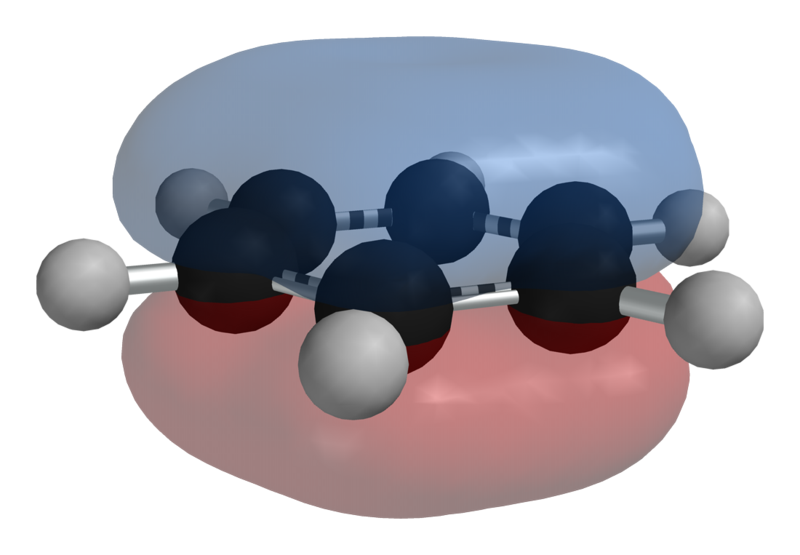
Pues bien; el furano tiene sus análogos heterocíclicos aromáticos para otros elementos del mismo grupo de la tabla periódica que el oxígeno, es decir, moléculas en las que el oxígeno del furano se ha sustituido por azufre, selenio y teluro. Así, encontramos el tiofeno (líquido incoloro de olor similar al del benceno), el selenofeno y hasta el telurofeno:
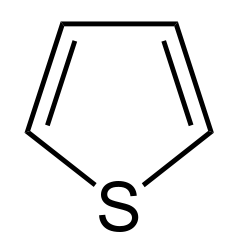
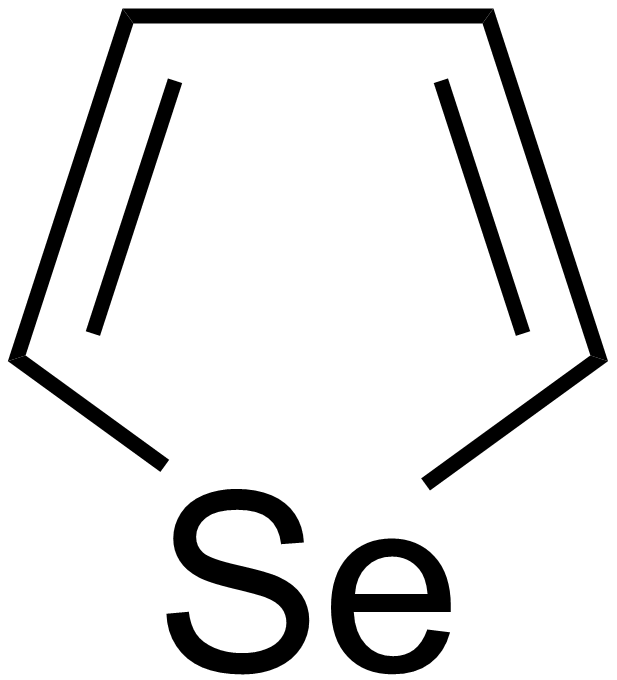

Aunque la geometría de estos anillos varía ligeramente con respecto a la del furano, así como su aromaticidad, por la distinta electronegatividad y tamaño de los heteroátomos, no deja de ser curioso hallar los mismo análogos como una serie química bien diferenciada de heterociclos de cinco átomos y dos insaturaciones alternadas. Son bonitos, ¿no?





Información Bitacoras.com
Valora en Bitacoras.com: Probablemente la mayoría de personas que hayan tenido un acercamiento a la química a nivel de bachillerato o de primer curso universitario habrá visto alguna vez este compuesto orgánico heterocíclico con oxígeno, el furano: E..…
Bitacoras.com, 11 Años Antes