Pirotecnia: las reacciones químicas de los fuegos artificiales
Escrito por Quimitube el 29 septiembre
Veíamos en una entrada reciente los compuestos químicos que producen los colores en los fuegos artificiales.
Como ya comentamos, toda mezcla pirotécnica debe contener una serie de componentes, esencialmente: oxidantes, reductores, estabilizantes o ligantes y agentes colorantes. Así, puesto que en las reacciones químicas de los fuegos artificiales hay agentes oxidantes y agentes reductores, en sentido amplio se pueden considerar como reacciones electroquímicas de oxidación y reducción. No obstante, se trata de reacciones redox en fase gaseosa, motivo por el cual no se pueden calcular los potenciales redox con los métodos habituales, ya que los potenciales estándar de reducción tabulados son válidos en disolución.
Los oxidantes proporcionan el oxígeno necesario para producir la combustión de la mezcla, y los más utilizados son los nitratos, los cloratos y los percloratos. Estos oxidantes, en su mayoría, producen reacciones fuertemente exotérmicas, a excepción del nitrato, que son las siguientes:
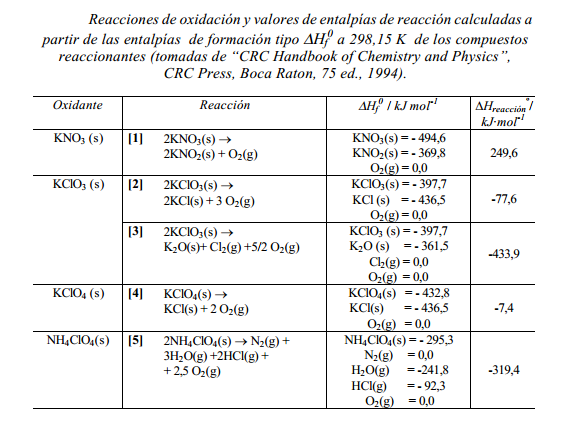
Reacciones de oxidación reducción en los fuegos artificiales. Tabla procedente de «Química de los fuegos artificiales: un recurso didáctico tomado de las fiesta populares». F. Peral y otros. UNED
Las reacciones exotérmicas, según el Principio de Le Chatelier, se favorecen a baja temperatura.
En cuanto a los agentes reductores, estos actúan como combustible reaccionando con el oxígeno producido por los oxidantes y, como consecuencia, se producen gases a alta temperatura.
Algunos de los reductores utilizados son el azufre y el carbono, que reaccionan con el oxígeno para formar dióxido de azufre (SO2) y dióxido de carbono (CO2) y que son, junto con el nitrato potásico o nitrato sódico (en proporciones de 10, 15, 75%) los componentes tradicionales de la pólvora negra.
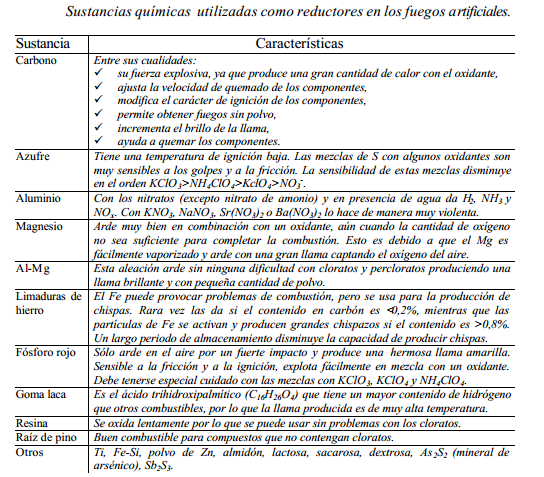
Sustancias químicas reductoras en los fuegos artificiales. Tabla procedente de «Química de los fuegos artificiales: un recurso didáctico tomado de las fiesta populares». F. Peral y otros. UNED
Además de los oxidantes y reductores, se adicionan otras sustancias que actúan como reguladoras de la velocidad de la reacción y como ligantes de la mezcla.
Así, se puede acelerar, o retardar, la reacción cuando se combinan dos agentes reductores; los metales se añaden a menudo para acelerarla y cuanto más fino es el polvo que se mezcla, más rápida es la reacción. Por su lado, los agentes ligantes deben tener, entre otras, las siguientes características: un fuerte poder de cohesión que permita la consolidación de la mezcla; resistencia al agua o a cualquier disolvente; dureza; estabilidad para no descomponerse durante el almacenaje; y, por último, no deben alterar el color de la llama del compuesto. El producto más usado como ligante es la dextrina, aunque también son muy utilizados la goma arábiga y el parlón (isopropeno de caucho clorado… ¡otra vez el isopreno!) que, además, es útil cuando se usan sales de estroncio y bario para obtener colores rojos y verdes.





[…] […]
Quimitube: una web ejercicios con mucha química | Triplenlace, 13 Años Antes
[…] Pirotecnia: las reacciones químicas de los fuegos artificiales […]
Química pirotécnica: base química de los fuegos artificiales | Quimitube, 12 Años Antes