Contenido del Vídeo
Hemos visto en el primer apartado de introducción a la termodinámica química el concepto de sistema y los tipos de sistemas termodinámicos existentes. Ahora bien, una vez delimitado un sistema termodinámico, ¿qué necesitamos conocer para definirlo en profundidad? Necesitamos conocer, además de la composición química del sistema, el valor de una serie de variables que determinan el estado del mismo desde un punto de vista macroscópico. A estas variables se las denomina Variables Termodinámicas. Algunos ejemplos de Variables Termodinámicas son: volumen, temperatura, presión…
Tipos de Variables termodinámicas: extensivas e intensivas
Las variables termodinámicas se clasifican en dos tipos, atendiendo a su dependencia o independencia con la cantidad total de materia presente en el sistema. Así, tenemos:
- Variables extensivas: si su valor depende de la cantidad o porción de sistema que se considera, por ejemplo: masa, volumen, número de moles…
- Variables intensivas: si su valor no depende de la cantidad de sistema considerado, por ejemplo: temperatura, densidad, presión, concentración…
Una forma sencilla de distinguir si una variable es extensiva o intensiva es dividir el sistema en dos bloques iguales y considerar si dicha variable cambia o se mantiene constante con respecto al sistema completo. Imaginemos que tenemos el siguiente sistema, constituido por 1 mol de hidrógeno en un recipiente de 22,4 litros:
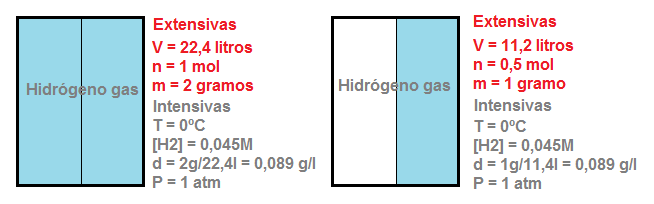
Aunque para el sistema anterior hemos indicado muchas variables, para describir por completo el estado de un sistema no es necesario conocerlas todas, se pueden limitar, dado que las variables termodinámicas se hallan relacionadas entre sí por ecuaciones matemáticas. Por ejemplo, la ecuación de Clapeyron para los gases ideales:
P·V = n·R·T
Donde:
P = presión (atm o pascales, Pa)
V = volumen (litros o m3)
n = número de moles
R = constante de los gases ideales, 0,082 atm·l/K·mol o 8,31 J/K·mol
T = temperatura en grados kelvin (K)
Dada esta ecuación para los gases ideales, bastará conocer la presión, el volumen y la temperatura para definir el estado del sistema, y el número de moles, o la densidad, o la masa, se podrían calcular conociendo dichos valores de P, V y T. Por tanto, con estas variables el sistema quedaría totalmente descrito.
Procesos isotermos, isobáricos, isocoros y adiabáticos
Un procedimiento habitual a nivel experimental para facilitar el estudio de los sistemas termodinámicos es limitar el número de variables de dicho sistema, manteniendo algunas fijas. Por ejemplo, si estudiamos un proceso a una temperatura constante de 25ºC, la temperatura dejará de ser una variable (no varía) y pasará a ser un valor numérico. Este tipo de proceso en el que se fija una variable adopta su nombre en función de cuál sea la variable fijada:
- A los procesos que se llevan a cabo a temperatura constante, se los denomina isotermos o isotérmicos (T = cte)
- A los procesos que se llevan a cabo a presión constante, se los denomina isobáricos (P = cte)
- A los procesos que se llevan a cabo a volumen constante, se los denomina isocoros (V = cte)
- A los procesos que se llevan a cabo sin transferencia de calor entre el sistema y el entorno, se los llama adiabáticos (Q = 0)
Definición de función de estado
Por último, aunque no por ello menos importante, debemos saber que algunas variables termodinámicas son, además, lo que se conoce como funciones de estado. ¿Qué significa esto? Significa que si el sistema sufre una modificación y pasa de un estado A a un estado B, el valor de estas variables termodinámicas que son funciones de estado no depende de cómo se ha efectuado la transformación, sólo del estado del sistema.
Veremos esto con un ejemplo concreto para que sea más sencillo, tomando como variable la temperatura. Consideremos un sistema que está en un estado A en el cual la temperatura es de 20ºC. Este sistema sufre una transformación y pasa a estar en un estado B en el cual la temperatura es de 60ºC. El sistema en le estado B seguirá estando a 60ºC independientemente del camino que haya seguido la transformación. No depende del camino que ha seguido dicha transformación, no importa si se ha calentado y luego enfriado, o si se ha calentado progresivamente… La temperatura en el estado B seguirá siendo de 60ºC, sin importar cómo se ha llegado a ello. Por esto, la temperatura es una función de estado, sólo depende del estado del sistema en el momento en que lo consideremos.
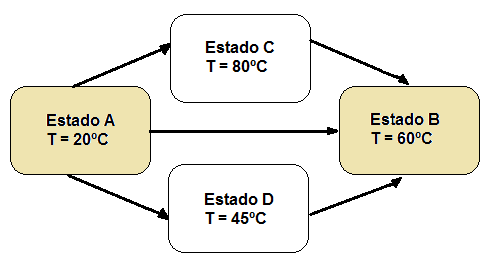
Otra forma de decir esto es que las variaciones que experimentan las funciones de estado sólo dependen del estado inicial y final del sistema. En nuestro caso la variación de temperatura es de 40ºC (60 – 20).
Otras variables termodinámicas que son función de estado son el volumen, la presión, y otros nuevos conceptos en los que vamos a profundizar a lo largo del tema como la energía interna, la entalpía, la entropía y la energía libre de Gibbs.
Category: Teoría de Termoquímica y Termodinámica Química.





 Estructura Atómica
Estructura Atómica Enlace Químico
Enlace Químico Termodinámica química
Termodinámica química Equilibrio Químico
Equilibrio Químico Ácido Base
Ácido Base Redox
Redox Selectividad
Selectividad
GRACIAS!
Me da curiosidad que gana esta pagina? o la chica de los videos? le pagan por las clases que hace? es solo curiosidad…
Como sea muchas Gracias, soy estudiante de Geología primer año y
aprobare mi Química I
gracias a ustedes 🙂
Belen, 12 Años Antes
Es posible tener los apuntes en pdf?
Felicidades por los videos.
Isidre Badia, 12 Años Antes
Son unos genios. Estoy preparando mi final de quimica general y esto me sirve muchisimo. Gracias desde Argentina, Misiones.
Andres, 12 Años Antes
Muchas gracias Andrés, ¡suerte con tu final de química!
QuimiTube, 12 Años Antes
Tengo una duda sobre termoquimica, ¿Por qué en una reacción p->r
si p se ha transformado casi por completo en r, AS sera igual tanto en un sentido como en el otro, (Ley de hess) ?
y ¿Por que si hay un numero igual de moles de reactivos que de productos AH=AE porque AS es cercano a 0?
Lidia, 12 Años Antes
¡Hola Lidia! La primera pregunta que formulas no la entiendo muy bien, lo siento… En cuanto a la segunda, solo será si hablamos de moles de gas. Si los moles de gas son iguales en reactivos y productos la entropía apenas variará, porque son los gases los que presentan una entropía mayor. Te sugiero que veas estos vídeos sobre entropía:
http://www.quimitube.com/videos/termodinamica-teoria-18-tercer-principio-de-la-termodinamica-entropia-molar-estandar/
http://www.quimitube.com/videos/termodinamica-teoria-19-1-como-calcular-la-variacion-de-entropia-de-una-reaccion-con-las-entropias-molares-estandar/
http://www.quimitube.com/videos/termodinamica-teoria-19-2-deduccion-cualitativa-del-signo-de-la-entropia-de-reaccion/
Un saludo
QuimiTube, 12 Años Antes
Gracias Quimitube.
Soy estudiante de bachillerato y esto no lo encontraba y me sera de mucha ayuda para mi examen de Física I
cintia, 12 Años Antes
Hola Cintia, muchas gracias por tu comentario, me alegra que te sirva. ¡Suerte con tu examen! Un abrazo
QuimiTube, 12 Años Antes
hola, excelente blog… me he visto todos los videos son muy explicativos, pero tengo una duda… y ya me la ha preguntado varias veces el profe pero la respuesta q le doy el siempre dice q no es… y ya la he buscado en todos lados y en todos lados dice lo mismo… la pregunta es: porque una funcion de estado solo depende de su estado inicial y final? mi respuesta a esto ha sido: porque sus valores dependen unicamente del estado en concreto del sistema y no del camino o transformaciones que halla sufrido para llegar a un estado….. no se si estoy mal.. pero eso lo he leido en todos lados hasta en los libros… me podrias ayudar con esto…??
mil gracias por tus videos y el blog me han sido de muchisima ayuda y eso que estoy en la universidad..!! besosss espero q me puedas ayudar!! 🙂
meli, 12 Años Antes
Hola Meli, muchas gracias por tu apoyo y por tu comentario. ¿Tu pregunta es si esa respuesta es correcta? A mí sí me parece una repuesta adecuada, ¿es que no te la dan por válida?
QuimiTube, 12 Años Antes
hola, si, la respuesta q estoy dando la a pregunta es correcta?? porque ya la he respondido de esa forma y el profe dice q no…!!! 🙁
no se si tiene q ser una respuesta mas tecnica, pero en todos lados hasta en los libros dice asi… no se si es q el profesor tiene otra visión de lo que es una función de estado o sera q la respuesta esta muy obvia y sencilla?? jajaajajaj!
mil gracias por responder 🙂
meli, 12 Años Antes
hola! me dieron el siguiente ejercicio y no puedo resolverlo
calcule la constante de equilibrio a 25°C y a 150!C utilizando los datos del apendice 2A
NH4Cl (s)—–NH3(g) + HCl(g)
GRACIAS!!! MUY BUENOS LOS VIDEOS!!!
SABRY, 11 Años Antes
¡Hola! Bueno, te recomiendo que veas los vídeos de equilibrio químico y que intentes hacerlo con ellos: http://www.quimitube.com/videoscategory/videos-equilibrio-quimico/
Además no sé qué datos vienen en el apéndice de tu libro… Un saludo grande y gracias por tu comentario.
QuimiTube, 11 Años Antes
Muchas gracias por los videos y los apuntes, me han sido de mucha ayuda tanto en química I como en química II 🙂
Jorge, 11 Años Antes
Muchas gracias a ti por comentar, me alegra mucho que te haya servido 🙂 Un saludo grande
QuimiTube, 11 Años Antes
Me enamorado de tus clases, que genial tu manera de explicar bastante claro los temas. Te agradezco infinitamente el aporte que nos haces.
Saludos.
daniel, 11 Años Antes
¡Muchas gracias Daniel!
QuimiTube, 11 Años Antes
Eres la mejor pedagoga (: , me ahuda mucho y eso que voy en la universidad, deberias contestar el problemario de el lobro FISICOQUIMICA de Caestellan.
Santos, 11 Años Antes
¡Hola Santos! Muchas gracias 🙂 No conozco ese problemario, pero si tengo ocasión de conseguirlo le echaré un vistazo para buscar ejercicios interesantes. Un saludo grande.
QuimiTube, 11 Años Antes
Buenos videos, muy bien explicados,, muy didácticos.
Carlos, 11 Años Antes
Muchas gracias Carlos, bienvenido.
QuimiTube, 11 Años Antes
me sirvio mucho gracias a ti estoy en 1ro en la secundaria y mi maestra quedo imprecionada y megane 100
gracias y que Dios te bendiga
angeles esther betancourt tejeda, 11 Años Antes
¡Enhorabuena por ese 100!
QuimiTube, 11 Años Antes
Excelente página!, muy buenos videos, ha sido de gran ayuda! Muchas gracias desde México D.F.
Abbey, 10 Años Antes
¡Hola! Mil gracias por tu comentario, un saludo grande hasta México D.F.
QuimiTube, 10 Años Antes
solo puedo decir excelente los vídeos, muy pedagógicos , didácticos… lo justo , a mi me fue de utilidad, reinicie los estudios a los 63 años, estoy en primer año de ing. en computación en la universidad de córdoba argentina, tengo química aplicada,después de 42 años que termine el secundario no recordaba casi nada de química,me fue de mucha ayuda los vídeos de termoquimica,..muchas gracias.
RODOLFO
Rodolfo, 10 Años Antes
solo puedo mandar un aplauso para ti y tu linda pagina deverdad que dices las cosas muy simples y sin mas complicaciones ( como debe ser jaja), la verdad contigo si me caso jajaja, un saludo desde mexico, felicitaciones y sigan así.
atte alex estudiante de ingenieria mecánica
ALEJANDRO, 10 Años Antes
Hola Alex, mil gracias por tu comentario, me has hecho reír 🙂 Me alegra mucho que las cosas te parezcan sencillas, es la base de todo aprendizaje (en mi opinión), simplificar lo complejo. Un saludo grande hasta México.
QuimiTube, 10 Años Antes
Y una pregunta mas por favor. La temperatura en un proceso isotérmico sigue siendo función de estado?
Edwin, 9 Años Antes
Muy buena la explicación de este tema que paresia complejo, la felicito. Una consulta la masa, numero de moles y la densidad pueden ser también funciones de estado? o que tendría que hacer para darme cuenta que si es una función de estado.
Edwin, 9 Años Antes
Y una pregunta mas por favor. En un proceso isotérmico la temperatura sigue siendo función de estado?
Edwin, 9 Años Antes
Gracias los videos y explicaciones me han de sido de gran ayuda, las temáticas desarrolladas, son claras y concretas, Felicitaciones.
ESPERANZA, 9 Años Antes
Muchas gracias Esperanza, ¡bienvenida!
QuimiTube, 9 Años Antes
Hola. Alguien sabría explicarme como obtener la ecuación diferencial para poder integrarla (eso ya lo hago yo) que me lleve a poder relacionar la p-T adiabáticamente?
Muchas gracias
MARCOS FRIGOLS GALAN, 9 Años Antes
Hola Marcos, lo siento lo que preguntas se escapa de mis conocimientos actuales, a ver si hay suerte y alguien que lo tenga más fresco te lo puede indicar. Un saludo.
QuimiTube, 9 Años Antes
Felicitaciones por el vídeo esta muy bien explicado el tema de Variables Termodinámicas, solamente desearía información para realizar la bibliografia correspondiente, gracias
Sergio Duque, 8 Años Antes