Producción de jabón casero: reacción de saponificación de grasas
Escrito por Quimitube el 30 agosto
Lo recuerdo como algo lejano, casi legendario, pero sé que mi madre me contó en alguna ocasión que, cuando ella era niña, fabricaban el jabón en casa. Para ello empleaban básicamente productos de desecho, como mantecas animales no útiles y aceites de freír usados. Lo «maceraban» con «barrilla» (hidróxido sódico, NaOH) y cuando el jabón espesaba, lo dejaban en reposo hasta que se separaba en varias fases, y una de ellas cuajaba lo bastante como para compactarlo y después cortarlo en forma de pastillas con un cuchillo. Después, las pastillas se dejaban endurecer hasta que estaban listas para su uso.
Las pastillas de jabón casero realizadas con aceite de oliva (no usado) tienen este aspecto:

- Pastilla casera de jabón de aceite de oliva
Pues bien, en esta entrada vamos a hablar de esta reacción química: la reacción de saponificación de las grasas para la producción de jabón.
¿Qué es un jabón químicamente hablando? Un jabón es un carboxilato procedente de un ácido graso, es decir, el ácido graso ha perdido su protón quedando como un anión (ácido graso, RCOOH, carboxilato, RCOO(-)) el cual podrá después combinarse con un catión metálico, generalmente un alcalino, como el sodio (Na+) o el potasio (K+) (dando RCOONa o RCOOK).
Por ejemplo, el acetato sódico, CH3COONa, es un carboxilato procedente de un ácido carboxílico, el ácido acético. El caso del jabón es semejante, pero el ácido carboxílico correspondiente es un ácido graso, lo cual quiere decir que, a diferencia del acetato que tiene únicamente 2 carbonos, este otro tiene una cadena de carbonos muy larga e hidrofóbica (desde 12 a 24 carbonos, generalmente).
A continuación puedes ver la estructura química de dos ácidos grasos, el ácido palmítico (componente del aceite de palma, el de coco, y también grasas animales como la mantequilla o la nada) y el ácido oleico (principal componente del aceite de oliva):
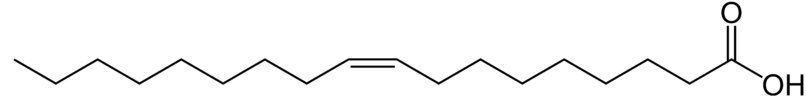
- Ácido oleico
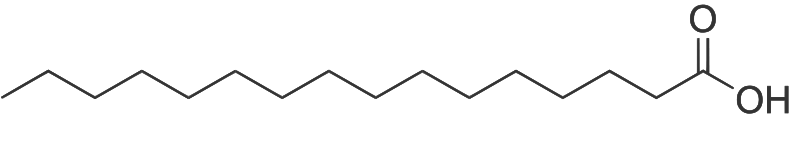
- Ácido palmítico
Así pues, los ácidos grasos son ácidos carboxílicos (contienen un grupo COOH) que pueden ser neutralizados con una base fuerte para dar jabón, según:
R-COOH (ácido graso) + BOH –> R-COOB (jabón) + H2O
Ésta sería, por tanto, de una reacción de neutralización ácido base muy sencilla.
Sin embargo, los lípidos que hallamos en la naturaleza y que empleamos para la fabricación casera de jabón, como los aceites vegetales o las grasas animales, no están en forma de ácidos grasos libres, sino principalmente como ésteres de ácidos grasos. En concreto, los aceites y las grasas son triglicéridos de glicerol o glicerina (1,2,3-propanotriol o propanotriol), ya que el glicerol es capaz de enlazar tres carboxilatos R-COO(-), por lo que reciben el nombre de triacilglicéridos o triglicéridos. Estos tres carboxilatos pueden ser distintos entre sí o iguales, y pueden ser saturados (todos los enlaces simples) o insaturados (con dobles y triples enlaces en su cadena).
A continuación puedes ver la estructura de un triglicérico y la estructura del glicerol o glicerina:
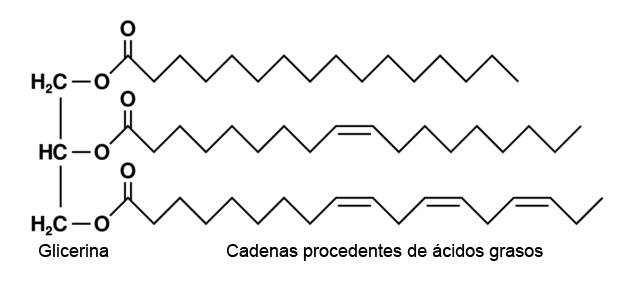
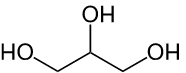 Glicerina
Glicerina
Es por este motivo, es decir, que hallamos las grasas en forma de triglicéridos, por lo que la reacción de las mismas con el álcali para dar jabón produce un subproducto, además del propio jabón, que es la glicerina, cuya estructura química acabamos de observar.
Así, la reacción de saponificación propiamente dicha será, por tanto:
Éster de ácido graso + BOH –> RCOOB (jabón) + Glicerina
Si nosotros queremos llevar a cabo esta reacción de saponificación en casa, debemos utilizar cierta cantidad de álcali, generalmente hidróxido sódico, NaOH, dependiente del tipo de grasa que empleemos. Cada grasa tiene un determinado índice de saponificación, que se define como los miligramos de KOH necesarios para saponificar un gramo de grasa.
No obstante, puesto que si usamos grasas de deshecho no es fácil determinar su índice de saponificación, se puede emplear una aproximación de 0,5 kg de sosa por cada 2,5 litros de grasa (si es sólida a temperatura ambiente, podemos medirla derretida).
Por si quieres intentarlo tú mismo, comentaré un procedimiento bastante general: mezclamos 2,5 litros de aceite usado (recuerda que el aceite usado es altamente contaminante y no debemos permitir que acabe en el mar o en los ríos) y 0,5 kg de sosa cáustica, NaOH (¡cuidado, que quema!), disuelta en agua. La disolución de NaOH en agua es fuertemente exotérmica, por lo que hay que ser cauteloso. También conviene añadir algo de sal a la mezcla, NaCl, para facilitar la separación de fases posterior.
Cuando se mezcla el aceite con la disolución de NaOH debes remover permanentemente y siempre en el mismo sentido. Además debes calentar la mezcla hasta ebullición y mantenerla de este modo durante dos horas aproximadamente. Con este calentamiento y este tiempo, se produce la reacción de saponificación que estamos buscando. Una vez que la mezcla ha espesado, debes pasarla a los moldes que hayas preparado y dejarla endurecer. Probablemente se vaya separando durante el endurecimiento otra fase acuosa, que contendrá hidróxido sódico que no haya reaccionado (en exceso) y también glicerina, y conviene irla separando. Antes de que solidique del todo debes cortar las pastillas, a no ser que hayas empleado moldes del tamaño de una única pastilla de jabón.
¿Te gusta el tema de los jabones caseros? ¿Quieres aprender sobre ellos y sobre cómo elaborarlos en mayor profundidad? Tal vez te sirvan estos libros:





Dios mi se me a vuelto un vicio visitar esta pagina, siempre quise hacer jabón casero.
wifredo suarez, 13 Años Antes
¡Gracias! 😀 Espero que si lo intentas te salga un buen jabón y, si no, al menos que te diviertas.
QuimiTube, 13 Años Antes
hola eres linda me gustan tus videos soy estudiante de ing quimica
Hermis, 13 Años Antes
Me alegro de que te gusten, espero que te sirvan de ayuda. La ingeniería química es muy interesante, al menos a mí me lo parece. Un saludo.
QuimiTube, 13 Años Antes
Hola, yo justamente acabé de hacer jabón hace dos días, pero el procedimiento que empleé fue diferente. Usé 180g de manteca, con 180g de NaOH disueltos en 600ml de agua, y utilicé alcohol pero que se disolviera la manteca y hubiera un mayor rendimiento de reacción, tuvimos un pequeña complicación pero al final si nos quedó una pasta que se enjuagó con agua fría para quitar el exceso de NaOH y los productos formados. Aun esperamos que se seque, sin embargo huele raro >.<! jajaja Un saludo, excelente página 🙂
Carlos, 13 Años Antes
¡Hola Carlos! Gracias por aportar tu receta, esperemos que cuando se seque huela un poco mejor jajaja, un saludo grande 🙂
QuimiTube, 13 Años Antes
Sigue oliendo un poco raro pero ya mucho menos x) Quisiera saber si de casualidad no me podrían decir como aromatizar un jabón, si es que hay aromatizantes que se le agreguen al jabón antes de compactarlo, y como en que tipo de tiendas lo podría conseguir, de antemano gracias. 🙂
Carlos, 13 Años Antes
Pues puedes agregar aceites esenciales de plantas y frutas, por ejemplo aceite esencial de rosas, de fresa, de limón, de naranja… también puedes poner las cáscaras en trocitos, sobretodo las de limón y naranja creo que te pueden quedar bien, y son fáciles de conseguir en muchas tiendas tanto de cosméticos como droguerías. Eso sí, es mejor que no los eches con el jabón caliente porque perderías parte de la cantidad agregada por evaporación.
QuimiTube, 13 Años Antes