Contenido del Vídeo
En este ejercicio de estructura atómica determinaremos diferentes estados de un mismo elemento químico a partir de distintas configuraciones electrónicas. Con diferentes estados nos referimos a saber discernir, en primer lugar, el estado fundamental y, después, otros estados importantes como el estado excitado o el estado ionizado y también aquellas configuraciones electrónicas que representan estados prohibidos porque, en verdad, no pueden darse por uno u otro motivo (principio de máxima multiplicidad de Hund, electrones antiparalelos en un mismo orbital…).
El enunciado completo del ejercicio es:
A continuación se muestran distintas configuraciones electrónicas para el átomo de nitrógeno:
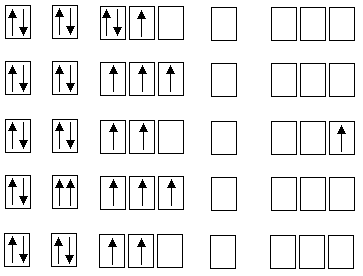
Indica cuáles corresponden a estados: excitado, fundamental, prohibido e ionizado.
Category: Estructura atómica y Estructura de la materia.
Etiquetas: Configuración electrónica.





 Estructura Atómica
Estructura Atómica Enlace Químico
Enlace Químico Termodinámica química
Termodinámica química Equilibrio Químico
Equilibrio Químico Ácido Base
Ácido Base Redox
Redox Selectividad
Selectividad
quisiera saver si los atomos exitados como el del azufre I Ne I 3s2 3p3 4s1 se puede escribir asi ? o tengo que entenderlo por el tema de hibridacion mescla de orbitales
giam pierrrs, 12 Años Antes
¡Hola! No hay ningún problema, lo puedes escribir así siempre y cuando sea un átomo libre. Si lo consideras enlazado a otros átomos como átomo central entonces sí que es posible que tengas que tener en cuenta sus hibridaciones.
QuimiTube, 12 Años Antes
A cual elemento pertenece esta figuracion electronica? Esta exitadoo 1s2 2s2 2p2 3d1
anonimo, 12 Años Antes
¡Hola! Como tienes un total de 7 electrones pertenece al nitrógeno.
QuimiTube, 12 Años Antes
Espero que no termines odiándome por pesada, jajaja. Es que me estoy volviendo loca con algunas cosas que estoy leyendo en el libro de texto sobre el estado excitado de los electrones. El libro dice textualmente «Estos estados excitados se corresponden con configuraciones en las que se han producido transiciones de electrones. Pero hay que destacar que las transiciones de electrones entre orbitales mencionadas únicamente son posibles dentro de un mismo nivel.». Después de eso ponen un ejemplo resuelto y dicen que la configuración 1s1 2s2 3s2 no es posible porque se promueven dos electrones de un nivel a otro y se saltan el nivel p. Lo que no entiendo es que diga que sólo puede haber transiciones dentro de un mismo nivel. Eso es absurdo, ¿no?
Ana, 12 Años Antes
En mi opinión tal vez sea un tanto desafortunado decirlo de este modo, ya que estrictamente todos los estados excitados deberían ser posibles. Ahora bien, sí que es cierto que los estados excitados dentro de un mismo nivel serán más probables, dado que requieren menos energía de excitación para producirse. Esto suele traducirse en líneas de mayor intensidad cuando hacemos el espectro de una sustancia en un espectrofotómetro, plasma o similiar. Sin embargo sí que es posible hallar líneas, y por tanto transiciones electrónicas, entre distintos niveles energéticos, sólo que son menos probables porque requieren una mayor energía.
Por tanto, creo que deberían matizar esto de «no es posible» por un «son más probables las transiciones entre el mismo nivel».
P.D.: Cómo voy a odiarte, me gusta mucho que la gente se tome en serio la química 😀
QuimiTube, 12 Años Antes
el nivel de energía son los nueros y las letras son subniveles.
entonces en ese orden de ideas, electrón saltaría a 3p, quedando en el mismo nivel de energía, pero en diferente subnivel (p)
Paula Andrea, 12 Años Antes
¡Hola! Sí, tienes razón, sería correcto decirlo de este modo. Un saludo.
QuimiTube, 12 Años Antes
Muchas gracias por aclararme la duda. Es que me da muchísima rabia encontrarme en los libros con cosas que me confunden y no me gusta dejarme cabos sueltos, quiero estar segura de que lo entiendo todo bien. 😀
P.D.: Creo que expreso el sentir general si digo que deberíamos… ¡hacerte un monumento!
Ana, 12 Años Antes
Es importante estar al tanto de cualquier detalle si quieres sacar la máxima nota, después, en el examen, algo que parecía muy simple o muy obvio puede ser la causa de perder un punto o incluso más. En cuanto a tu P.D.: jajajajajaja, ¡no es para tanto!
Un saludo muy grande
QuimiTube, 12 Años Antes
Hola! necesitaria tu ayuda para resolver un ejercicio. El ejercicio me dice: Indicar cuáles de estas configuraciones electrónicas corresponden al átomo en estado excitado, cuáles son imposibles y cuál representa a su estado fundamental:
a) 1s1 1p3
b)1s2 2s1 2p2
c)1s1 2s3
d)1s2 2s1 2p1 2d1
e)1s2 2s2 2p1
f)1s1 2s1 2p3
g)1s2 2s2
Agradezco mucho tu tiempo!
Denise, 12 Años Antes
Hola Denise, ¿has visto con detenimiento este vídeo? Con él debería darte una pista. Te oriento un poco: el apartado a es imposible porque en el nivel 1 no hay orbitales p. El segundo, por ejemplo, debería ser 1s2 2s2 2p1, por lo que al ser 1s2 2s1 2p2 significa que un electrón ha promocionado desde el orbital 2s a un orbital 2p, lo cual implica que en este caso se trata de un estado excitado. Con los demás puedes hacer lo mismo: el 3 excitado, el d doblemente excitado… Los apartados e y g corresponden a configuraciones fundamentales.
QuimiTube, 12 Años Antes
Hola , con el mismo N Z =7 , se podría dar este caso , 1s2 2s2 2p2 3s1 , yo creo que esta excitado , estoy en lo correcto ?
Alberto, 12 Años Antes
Hola muy bonita tu, y muy buenos tus videos, estan re bien explicados….Queria preguntarte que en el caso que algun ejercicio no nos den esos cuadraditos con los espines de los electrones, que solo nos den la configuracion electronica, por ejemplo:
1s2 2s2 2p5 3s1
en ese caso es facil identificar que esta en un estado exitado por que salto un electon del subnivel 2p5 al subnivel 3s. Ahora MI PREGUNTA ES ¿Pero como haria en otro caso?
Muchas gracias!! espero haber sido claro con la pregunta
Saludos desde argentina!
Maxi, 12 Años Antes
Hola, ¿me podría resolver una duda de un ejercicio?. Le cuento:
Pide razonar si la siguiente configuración electrónica corresponde a un estado fundamental, excitado , o no es posible:
1s2 2s1 2p6 3d2
En el solucionario de mi libro aparece que corresponde a un estado excitado, pero me ha causado duda por el 2s1, que pienso que no puede ser, y ando bastante liada con esto.
Le agradecería mucho si me lo aclarara.
Un saludo y gracias.
Mª Ángeles, 12 Años Antes
Hola Mª Ángeles, aunque resulte bastante raro sí que podría corresponder a un estado excitado. Lo que ocurre es que es un estado muy poco probable, ya que la configuración electrónica adecuada para 11 electrones sería: 1s2 2s2 2p6 3s1. Así, habría saltado un electrón del 2s al 3d (lejísimos) y otro electrón del 3s1 también al 3d, para darte finalmente 1s2 2s1 2p6 3d2. No podemos decir que sea prohibida, sino excitada, pero sí que es una configuración prácticamente imposible de lograr por parte de un átomo.
QuimiTube, 12 Años Antes
quiero que me expliques cómo se hace la configuración electrónica de los diferentes estados del átomo
MANUELA, 12 Años Antes
¡Hola! Viendo este vídeo con detenimiento te irá bien para tus ejercicios. Un saludo.
QuimiTube, 12 Años Antes
Hola, tengo un par de dudas sobre la configuración electrónica y la AE y EI.
La primera: la primera energía de ionización de un átomo excitado sería mayor o menor que la de ese átomo en estado neutro? Ejemplo: 1s2 2s2 3s1. Yo diría que en este caso disminuiria porque el último electrón está en el nivel 3, pero en el libro pone que sería mayor porque el electrón se encuentra en un nivel más energético, y eso es cierto, pero que yo sepa la EI no depende tanto de la energia del orbital y la n como de la distancia al núcleo. Es que según eso el Na tendria mayor EI que el S x ejemplo porque su último electrón es 3s1 y el del azufre 2p4 si no recuerdo mal, cuando siempre se dice que al bajar en el periodo la EI baja.
¿Hay alguna regla para saber si la AE es de un metal o un no metal? En un ejercicio me dan una positiva, 1.62 eV, y otra negativa, -3.14 eV, y me dice que la negativa es de un metal porque liberan energía al captar un electrón y la positiva de un no metal. ¿Por qué? ¿No sería al revés? Si se supone que los metales tienden a perder electrones de su ultima capa y los no metales a ganarlos…
Muchas gracias y un saludo!!
Rubén, 12 Años Antes
¡Hola Rubén!
Es curioso, ambas cosas que indicas que pone tu libro me parece que están al revés. La energía de ionización será inferior en el átomo excitado, porque ya hemos aportado cierta cantidad de energía de la necesaria para arrancar el electrón. Así, será necesaria menos energía para acabar de ionizar el átomo, por lo que su EI será inferior. En cuanto a la afinidad electrónica, son los no metales los que emiten energía cuando captan un electrón (o mayor cantidad de energía) por lo que el valor de -3,14 eV sería el del no metal, tal y como tú comentas.
Un saludo,
QuimiTube, 12 Años Antes
me surge una duda, en el estado excitado cuando dices que al electrón le falto energía para para quedarse en 2p2 y no pasar al 3p1, no seria lo contrario? absorbió un cuanto de energía mayor por eso pasó a un estado mas avanzado y no se quedó en el orbital 2p2?
Esteban, 11 Años Antes
Hola Esteban, efectivamente si he dicho eso (no me ha sido posible revisar el vídeo ahora) estaría mal. Cuando el electrón está en un estado excitado es porque ha absorbido mayor energía para pasar al mismo. Un saludo y gracias por tu comentario.
QuimiTube, 11 Años Antes
Un atomo x tiene la siguiente configuracion electrpnica: 1s2 2s2 2p6 3s2 3p6
Hallar Z,A,n°
camilo, 11 Años Antes
Hola, Camilo, no entiendo tu comentario… ¿Es acaso una pregunta?
QuimiTube, 11 Años Antes
Hola. Me puedes explicar muy detalladamente porque un un orbita p hay como maximo 6 electrones? Y tambien como saber si una molecula es polar o apolar. Gra6
Luisa Romero, 11 Años Antes
Hola Luisa, en todos los orbitales solo caben 2 electrones. Lo que ocurre es que como en un mismo nivel hay 3 orbitales p, al caber 2 electrones en cada uno son 6 en total. En cuanto a la polaridad, tienes este vídeo:
http://www.quimitube.com/videos/enlace-covalente-polaridad-de-enlace-y-polaridad-molecular
Si no tienes una buena base teórica te sugiero que veas los vídeos de teoría antes de ver estos otros de ejercicios, o que lo veas en este orden:
http://www.quimitube.com/videoscategory/enlace-quimico
Un saludo
QuimiTube, 11 Años Antes
Cual elemento sería 1s² 2s¹ 2p⁴ en estado excitado?
Anonimo, 11 Años Antes
Hola, debes contar el número total de electrones. Como son 6, se trata del carbono.
QuimiTube, 11 Años Antes
Puede existir esta configuracion de estado exitado? 2s2 2p2.. yo pienso q seria un esrado imposiblee..
silvia barcaya, 11 Años Antes
Hola Silvia, ¿te refieres a que el nivel 1s esté vacío? Yo creo que lo puedes plantear a nivel teórico, pero en realidad lo más lógico sería tener 1s2 2p2, por ejemplo, ya que la diferencia energética es menor y se daría ese salto antes que un salto del 1s al 2p.
QuimiTube, 11 Años Antes
Ósea que cuando un electrón es fundamental queda al final de la configuración electrones desapareados?
Ariana, 10 Años Antes
Hola Ariana, no tiene porqué, puedes tener átomos en cuya configuración fundamental no queda ningún electrón desapareado, por ejemplo los gases nobles.
QuimiTube, 10 Años Antes
hola hola, disculpa tengo una duda, a cual elemento correponde la configuracion electronica 1s2 2s2 2p2
y me da estas opciones
A- boro
B- flour
C- carbonato
D- oxigeno
E- Nitrogeno
porfavor ayudaaaaa!
guadalupe, 10 Años Antes
Hola Guadalupe, te sugiero hacer lo siguiente: sumando los valores de los electrones que hay en los orbitales de tu configuración, 1s2 2s2 2p2, es decir, 2 + 2 + 2, te da que tienes 6 electrones. ¿Qué elemento tiene 6 electrones de tu lista? Esto lo puedes mirar en la tabla periódica.
QuimiTube, 10 Años Antes
Como logra pasar un electrón del estado fundamental al estafo editado??
Soraya, 9 Años Antes
Cuando se le irradia con energía de la longitud de onda adecuada el electrón puede «saltar» de una órbita a otra superior, a un estado excitado (no editado).
QuimiTube, 9 Años Antes
Hola. Como puedo pasar el N2 a un estado excitado??
Paula, 9 Años Antes
¡Hola Paula! Tendrías que excitar las moléculas con una radiación de la longitud de onda adecuada, es decir, con una longitud de onda que coincida con alguna de sus transiciones electrónicas, aunque no sé cuáles son estos valores. Un saludo.
QuimiTube, 9 Años Antes
hola. cual serie el estado excitado para el mercurio
nicolas, 9 Años Antes
Hola, tendrías que poner un electrón de la capa de valencia en el orbital siguiente según el diagrama de Moeller. Un saludo.
QuimiTube, 9 Años Antes
Cual seria la configuración excitada del Vanadio?
Didier, 9 Años Antes
¡Hola! Tendrías que poner un electrón de la capa de valencia en el orbital siguiente según el diagrama de Moeller.
QuimiTube, 9 Años Antes
gracias fuiste de mucha ayuda
nicolas, 9 Años Antes
De nada, me alegra que te sirviera. Un saludo.
QuimiTube, 9 Años Antes
Cual seria la configuración electrónica excitada del paladio?por fa
Ivan, 9 Años Antes
Como he respondido a otros compañeros debes plantear la configuración electrónica y uno de los electrones de la última capa lo pones en un orbital superior… Un saludo.
QuimiTube, 9 Años Antes
hola cual sería la del radón?
Carlos, 9 Años Antes
Siempre procedes del mismo modo, un electrón de la última capa ha de ocupar un orbital superior y tendrás una configuración excitada.
QuimiTube, 9 Años Antes
Perdon la Conf electronica excitada del Radón
Carlos, 9 Años Antes