Contenido del Vídeo
Los compuestos covalentes son un grupo muy amplio, y en ellos hallamos 2 grupos de compuestos bien diferenciados, que presentan, además, propiedades prácticamente opuestas.
Por una parte, tenemos las sustancias covalentes moleculares, lo cual implica que están formadas por moléculas independientes. Por ejemplo, si consideramos el cloro gaseoso, diatómico, Cl2, los dos cloros están unidos entre sí por un enlace covalente fuerte (enlace intramolecular, dentro de la propia molécula). La estructura de Lewis para la molécula es:
![]()
No obstante, si tenemos un recipiente con una cierta cantidad de cloro gaseoso, tendremos moléculas individuales que no forman enlace químico. Entre ellas únicamente se establecerán unas fuerzas de carácter débil, llamadas fuerzas intermoleculares, que veremos en profundidad en un posterior apartado.
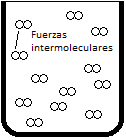
Cabe destacar que, aunque estas sustancias covalentes moleculares se unan entre sí por fuerzas intermoleculares de carácter débil, existen a temperatura ambiente en los tres estados de agregación: gaseosas (F2, N2, O2…), líquidas (agua, Br2…) y sólidas (glucosa, I2…).
Por otra parte, tenemos otro tipo de sustancias covalentes, que no están formadas por moléculas individuales sino que son macromoléculas, es decir, grandes redes cristalinas formadas por una infinidad de átomos unidos fuertemente entre sí mediante enlace covalente. Éstas son las redes covalentes o cristales covalentes. La estructura es generalmente ordenada y muy definida, y en ellas hallamos ejemplos naturales como son el grafito y el diamante (dos formas alotrópicas del carbono puro) o la sílice (SiO2). Dada la fortaleza de los enlaces que establecen la redes covalentes, siempre son sólidas a temperatura ambiente y, de hecho, presentan puntos de fusión y ebullición elevadísimos.
A continuación exponemos un breve esquema de los tipos de compuestos covalentes:
- Sustancias covalentes moleculares. Formadas por moléculas individuales.
- Gaseosas a temperatura ambiente: F2, N2, O2, Cl2, CH4…
- Líquidas a temperatura ambiente: H2O, CH3CH2OH (etanol), CH3COOH (ácido acético), Br2…
- Sólidas a temperatura ambiente: I2, glucosa, naftaleno…
- Cristales covalentes o redes covalentes. Sólidos formados por n átomos.
- Formadas por el mismo elemento: diamante, grafito…
- Formadas por varios elementos: sílice (SiO2), carburo de silicio o carborúndum, SiC…
Category: Enlace Químico y Teoría de Enlace Químico.
Etiquetas: Enlace covalente.





 Estructura Atómica
Estructura Atómica Enlace Químico
Enlace Químico Termodinámica química
Termodinámica química Equilibrio Químico
Equilibrio Químico Ácido Base
Ácido Base Redox
Redox Selectividad
Selectividad
Buenos dias,me encanto la explicacion de enlace químico,quisiera saber,si no es mucha molestia,que explicase algo de compuesto de coordinación,acerca de la nomenclatura de los complejos y isómeros que presentan. Saludos Cordiales.
Luciana, 8 Años Antes