Parafina líquida para calentar el hogar
Escrito por Quimitube el 20 enero
Cuando llega el invierno, sin duda es una prioridad para todos los hogares tener un método adecuado de calefacción sin que ello nos cueste una fortuna. No sé si será el método más económico (aunque al precio que está la electricidad seguramente será mucho más barato que poner placas calefactoras o aparatos de aire acondicionado), pero hace unos años adquirí una estufa de parafina pequeñita pero matona, tal que esta:

Estufa de encendido eléctrico que funciona con parafina líquida
La verdad es que estoy contenta, ya que la velocidad a la que es capaz de calentar una estancia es bastante sorprendente y permite seleccionar la temperatura. El combustible que utiliza es un líquido de olor penetrante, como de gasolina, que se vende en garrafas de distintos volúmenes, generalmente 20 litros. A continuación podéis ver una imagen de la etiqueta en la que se observa el contenido y las normas de seguridad:

Contenido y normas de seguridad de la parafina líquida
Puesto que no acaba de apreciarse bien, transcribiré lo que indica: «Contiene: hidrocarburos, C11-C14, isoalcanos, cíclicos, <2% aromáticos; hidrocarburos, C10-C13, n-alcanos, isoalcanos, cíclicos, <2% aromáticos.»
Como podéis ver no se trata de un único compuesto, sino un popurrí bastante considerable de diversos compuestos orgánicos formados por carbono e hidrógeno, con distinta longitud de cadena y distinta disposición de sus átomos. De esta forma, no podemos plantear una fórmula química para la parafina líquida sino que será una mezcla de hidrocarburos líquidos cada uno de ellos con su propia fórmula, de modo que es habitual escribir una fórmula genérica como esta:
Fórmula de la parafina líquida: CnH2n+2
Y así podemos escribir la reacción de combustión ajustada como:
![]()
Es decir, escribir la fórmula como si todos los compuestos que contiene fuesen n-alcanos, cadenas de carbono lineales sin enlaces dobles ni triples. Por ejemplo, si consideramos los que están indicados como C10-C13 (sí que estarán presentes porque pone n-alcanos en la etiqueta, es decir, de cadena abierta):
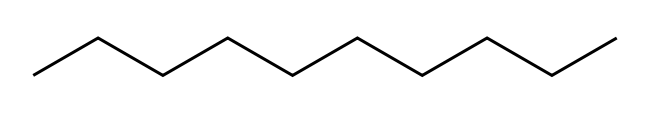
Estructura química del n-decano, n-alcano de 10 átomos de carbono, con fórmula C10H22
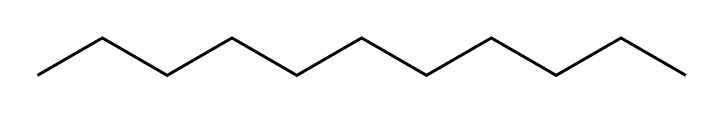
Estructura química del n-undecano, n-alcano de 11 átomos de carbono, con fórmula C11H24
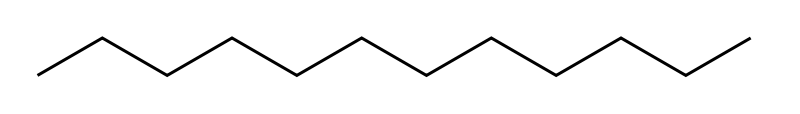
Estructura química del n-dodecano, n-alcano de 12 átomos de carbono, con fórmula C12H26
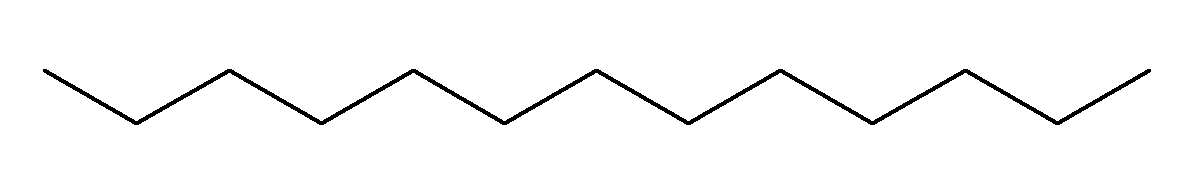
Estructura química del n-tridecano, n-alcano de 13 átomos de carbono, con fórmula C13H28
Para los que no estéis familiarizados con esta forma de representar los alcanos, cada vértice representa a un átomo de carbono y cada línea a un enlace. Los átomos de carbono del interior de la cadena están unidos a dos átomos de hidrógeno, que se omiten, y los dos del extremo de la cadena están unidos a tres átomos de hidrógeno, también omitidos. Todos ellos son líquidos inflamables y gran poder calorífico, lo que hace que sean útiles como combustibles (entalpía de combustión estándar de -6777 kJ/mol para el n-decano), además de permanecer en estado líquido en un rango de temperatura muy elevado (entre -28ºC y 174ºC para el n-decano).

Tabla: entalpías estándar de combustión de los n-alcanos desde C10 a C13
Las entalpías estándar de combustión de estos compuestos son muy elevadas, especialmente si tenemos en cuenta que los valores para el propano es aproximadamente de -2200 kJ/mol y para el butano de -2900 kJ/mol. No obstante, sus mayores masas moleculares harán que, si consideramos el poder calorífico por gramo de combustible, la diferencia no sea tan elevada sino similar, o incluso un poco menor para los hidrocarburos de cadena lineal larga.
Sin embargo, como indica en la propia etiqueta de la parafina líquida, no tenemos únicamente cadenas lineales, sino también «isoalcanos», término dentro del que se engloban diversos isómeros en los que compuestos con ese mismo número de carbonos se enlazan de forma distinta, presentando ramificaciones, o «cíclicos» es decir, compuestos con estructura cerrada. Por ejemplo, para el n-decano que hemos visto anteriormente, podríamos tener los siguientes.
Estructura química del ciclodecano, de fórmula C10H20
Aunque en realidad la cantidad real de compuestos en esta parafina líquida será inmensa. Solo el n-decano puede presentar hasta 75 isómeros distintos. Imaginad lo que pasará cuando tenemos en cuanta todas las posibilidades de todos los compuestos de C10 hasta C14, la cantidad de combinaciones de átomos de carbono es realmente abrumadora, por lo que la información que se indica en la etiqueta es en verdad bastante limitada. Así, lo que tenemos es una mezcla bastante amplia de hidrocarburos que se obtienen en la industria del petróleo, como subproductos en la fabricación de combustibles para automóviles.
La estufa previamente indicada tiene un consumo de entre 0,08 litros y 0,31 litros por hora de funcionamiento (dependiendo de la potencia, es decir, de la temperatura elegida) y, por tanto, una garrafa de 20 litros, que tiene un coste de 45 euros, podría durar entre 65 y 250 horas. Considerando que únicamente se utiliza de forma puntual cuando uno se encuentra en el interior de la estancia, creo que resulta bastante asequible.






Información Bitacoras.com
Valora en Bitacoras.com: Cuando llega el invierno, sin duda es una prioridad para todos los hogares tener un método adecuado de calefacción sin que ello nos cueste una fortuna. No sé si será el método más económico (aunque al precio que está la elect..…
Bitacoras.com, 11 Años Antes