Contenido del Vídeo
En función de su conductividad eléctrica, los sólidos se pueden clasificar en tres grupos: aislantes, conductores y semiconductores. Esta última propiedad, la semiconductividad, no puede ser explicada a partir del modelo del mar de electrones visto hasta ahora para el enlace metálico. Se requiere una teoría más profunda que es la teoría de bandas la cual, además de explicar la semiconductividad, explica también por qué los metales son muy buenos conductores de la electricidad.
Consideremos el metal litio, cuya configuración electrónica es:
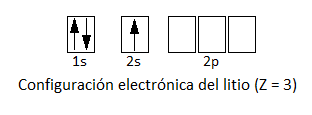
Vemos que un átomo de litio presenta un orbital 1s lleno (con 2 electrones) y un orbital 2s semilleno (con 1 electrón). También podemos considerar a efectos prácticos los orbitales 2p, que estarán en la capa de valencia del litio, aunque vacíos.
Pues bien, la Teoría de bandas considera que los orbitales atómicos de valencia de los N átomos del litio que estarán formando enlace metálico, se combinan entre sí para dar unos orbitales moleculares, pertenecientes a todo el cristal y con energías muy semejantes entre sí. Tan cercanos se hallan energéticamente estos orbitales moleculares formados, que decimos que dan lugar a una banda. Se obtienen tantos orbitales moleculares como orbitales atómicos se combinen.
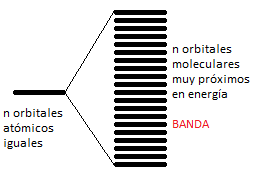
(Nota: estrictamente no es del todo correcto, o al menos no es la terminología más precisa, hablar de orbitales moleculares en compuestos sólidos. No obstante, en este curso lo trataremos de este modo por ser sencillo y más intuitivo que el solo concepto de «banda de energía»).
Así, si tenemos N átomos de litio, tendremos N orbitales atómicos 2s que darán lugar a N orbitales moleculares que podemos llamar también 2s por facilidad de comprensión. Estos orbitales estarán muy próximos en energía y darán una banda 2s. Lo mismo sucederá con los orbitales 3N 2p de los N átomos de litio (cada átomo de litio tendrá 3 orbitales 2p, px, py y pz), aunque estén vacíos, dando lugar también a una banda 2p.
A la banda formada por los orbitales 2s semillenos se le llama banda de valencia. A la banda vacía formada por los orbitales 2p, se la llama banda de conducción.
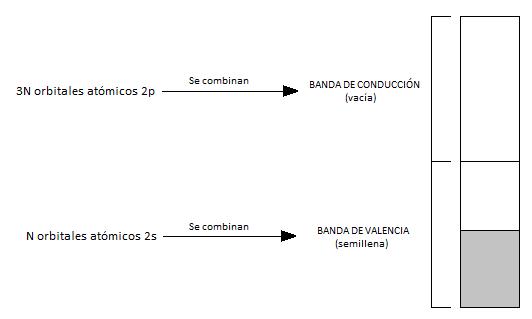
Por tanto, en los metales, hay bandas de valencia, que son bandas en las que se hallan los electrones de valencia y pueden estar llenas o semillenas, dependiendo de la configuración electrónica del metal, y bandas de conducción, que pueden hallarse vacías o parcialmente vacías y facilitan la conducción porque son energéticamente accesibles. De hecho, los metales son conductores porque las bandas de valencia y de conducción se superponen, y esto hace que los electrones se muevan con libertad de una a otra.
En el caso de los semiconductores, las bandas de valencia y de conducción no se superponen, pero la diferencia energética entre ambas es pequeña, por lo que una pequeña aportación energética hará que puedan promocionar electrones a la banda de conducción y, por tanto, conducir la corriente eléctrica.
En los aislantes, por su parte, las dos bandas están tan alejadas que la banda de conducción es inaccesible, motivo por el cual son incapaces de conducir la corriente:
![]()
Category: Enlace Químico y Teoría de Enlace Químico.
Etiquetas: Enlace metálico.





 Estructura Atómica
Estructura Atómica Enlace Químico
Enlace Químico Termodinámica química
Termodinámica química Equilibrio Químico
Equilibrio Químico Ácido Base
Ácido Base Redox
Redox Selectividad
Selectividad
hola!! muy didactico el resumen que realizaste…menos mal q lei antes de ver el video..sino estaba dificil de concentrarme viendot en el video jajaj saludos
guille01, 12 Años Antes
Gracias Guille, me alegro que te sirviera, bienvenido 🙂
QuimiTube, 12 Años Antes
Muchas Gracias por los videos,la verdad que asi se aclaran muchas cosas..admiro tu forma de expresarte..saludos!!
Gustavo, 12 Años Antes
Gracias Gustavo y bienvenido 🙂 Agradezco que te hayas tomado un tiempo para comentar porque anima mucho a continuar y me alegro mucho de que los vídeos te resulten de ayuda. Un saludo, Carmen.
QuimiTube, 12 Años Antes
Muy bueno el video la verdad es que esta muy bien explicado 🙂
Un saludo y gracias ! 😀
david, 12 Años Antes
Hola David, bienvenido, y gracias por comentar, me alegro de que te sirviera 🙂
QuimiTube, 12 Años Antes
Muchiiiiiiiiisimas gracias! Tanto por este video como por los demás. Mi nivel de química es nulo y la página me está ayudando mucho. Ahora hasta me veo con posibilidades de aprobar la asignatura!
Besos
Vi, 12 Años Antes
¡Hola Vi! Bienvenida 🙂 Me alegro de que te sirvan, verás como sí que apruebas, mucho esfuerzo, un empujoncito de quimitube y nada de desanimarse jejeje. Un abrazo.
QuimiTube, 12 Años Antes
gracias por los vídeos…no entendía la química pero ahora si y tengo la esperanza de aprobar.
karen, 12 Años Antes
Hola Karen, verás como sí que apruebas, y hasta con nota 🙂 Espero que la química te empiece a gustar, aunque sea un poquito. Un saludo grande.
QuimiTube, 12 Años Antes
Caramba.. pero de verdad muchas muchas gracias!!
Jesus, 12 Años Antes
Hola Jesús, me alegro de que te sirviera 🙂
QuimiTube, 12 Años Antes
Saludos, excelente tarea la que realizan, mucho éxito y gracias por compartir el conocimiento
Juan Antonio Arízaga, 12 Años Antes
Hola Juan Antonio, bienvenido. Muchas gracias por el apoyo y por el comentario, se agradece muchísimo 🙂
QuimiTube, 12 Años Antes
Es una pasada como te explicas! Sigue subiendo cosas a la página y nos salvaras a muchos de nosotros!! Un saludo 🙂
Sara Carnota, 12 Años Antes
Hola Sara, ¡gracias! Me encantará salvaros o mejor aún, ayudaros a sacar una notaza jejeje. Pronto subiré cosas nuevas, o eso espero. Un saludo y bienvenida.
QuimiTube, 12 Años Antes
sos una genia..!! tengo q rendir un final y con los videos que subis tengo mucha esperanza de aprobar y me esta empezando a gustar la quimica!!!!!!:-)
julieta, 12 Años Antes
Gracias Julieta y bienvenida. Me alegro muchísimo de que te estén yendo bien para aprobar y sobretodo de que te empiece a gustar la química, es muy bonito eso que dices 🙂
QuimiTube, 12 Años Antes
genial! muchísimas gracias lo entendí al momento hoy rindo el final de química y me estoy comiendo uno a uno tus vídeos!
Leandro, 12 Años Antes
¡Hola Leandro! Muchísima suerte con tu final, ¡ánimo!
QuimiTube, 12 Años Antes
Hola entendí todo el vídeo pero ¿Como hago para calcular la energía que necesita un electrón para pasar de una banda a otra en un semiconductor o un aislante?
daniel, 12 Años Antes
Hola Daniel, para calcular la energía necesaria para una transición electrónica siempre necesitas saber los niveles de energías medias de dichas bandas o la frecuencia de la transición (aunque no sé cómo se haría en la práctica para un semiconductor o asilante). Sabiendo dichos valores, entonces podrías calcularlo como por ejemplo aquí:
http://www.quimitube.com/videos/calculo-energia-transicion-electronic/
http://www.quimitube.com/videos/calculo-longitud-de-onda-serie-de-balmer-espectro-emision-hidrogeno/
QuimiTube, 12 Años Antes
Hola, en verdad me ayudo mucho el video para entender esta teoria tengo una expo sobre este tema y me ha sido de grandisima ayuda GRACIAS!!!!1
Ricardo, 12 Años Antes
Me alegro mucho, mucha suerte en tu exposición. Un saludo.
QuimiTube, 12 Años Antes
gracias 🙂
gabriel, 12 Años Antes
De nada 🙂
QuimiTube, 12 Años Antes
q linda!! que bueno que te des un tiempo para enseñar virtualmente, porque ayudas infinitamente a eliminar muchas dudas, tu método de enseñanza es genial 🙂 gracias .
Paola, 12 Años Antes
Mil gracias Paola, cuánto te agradezco tu comentario 🙂 Un saludo muy grande y bienvenida.
QuimiTube, 12 Años Antes
Hola, muy buenos tus videos, pero tengo algunas consultas que espero que me respondas 🙂
-En el primer ejemplo que hiciste del Na consideraste al siguiente nivel en la configuración (3p) y este seria una banda de conducción por tener orbitales vacíos. Sin embargo cuando diste el ejemplo del Al, su configuración termina en 3p1 y tu lo consideraste como banda de conducción, pero por qué no se podría considerar al siguiente nivel, osea al 4s2 como banda de conducción con orbitales vacíos?
– mi otra duda es por qué los orbitales 2s en el Na están próximos de energía y forman una banda ?
carolina, 12 Años Antes
¡Hola Carolina! Lo que ocurre es que cuando cambiamos de nivel ya suelen estar demasiado alejados energéticamente, por este motivo los orbitales 4s del aluminio están energéticamente muy lejos de los orbitales 3p, y por este motivo no hay conducción en dicho orbitales en este metal. De hecho esto es lo que ocurre en semiconductores y no metales, que los orbitales siguientes están lejos porque son de niveles posteriores. Otra cosa sería la diferencia entre por ejemplo los 3s y los 3p, que no es tan grande. En cuanto a la otra duda, en general siempre es así en los metales y esta es la base de la teoría de bandas, los orbitales de valencia del metal se combinan para formar orbitales moleculares que forman parte de todo el cristal, aunque no te sé explicar exactamente por qué con palabras sencillas. En cuanto a que estén próximos en energía los 2s de los sodios, es razonable porque todos son átomos de sodio idénticos, de forma ideal todos los orbitales 2s de todos los sodios tienen que tener la misma energía.
QuimiTube, 12 Años Antes
Hola! Exactamente era mi duda con respecto al aluminio. Entiendo que el espacio libre de la banda que forman los orbitales 3p, la cual estaría semillena, sera suficiente para que los electrones deambulen y se den las características metálicas del aluminio. ?Es correcta esa conclusion? Infinitas gracias por la ayuda.
Luis, 9 Años Antes
Hola Luis, sí, podríamos decirlo así, el aluminio tiene espacio en la banda de valencia suficiente para que «deambulen» a sus anchas y por tanto conduce la electricidad. Un saludo y gracias a ti por tu comentario.
QuimiTube, 9 Años Antes
Muy buena explicación!!!
Bertha Escárcega Vargas, 12 Años Antes
¡Gracias! 😀
QuimiTube, 12 Años Antes
Hola, la verdad que lamento no haber encontrado estos videos antes, mañana rindo y me estan sirviendo un monton! Muchas gracias, se entiende muy bien como explicas, segui asi. exitos
Santiago, 12 Años Antes
Hola Santiago, bienvenido. Espero que te fuese muy bien tu examen. Un saludo grande.
QuimiTube, 12 Años Antes
muy bueno el aporte! Soy estudiante de ing.quimica en unos dias rindo un parcial de inorganica y este tema lo dan asi nomas y quedan huecos,los cuales estoy tapando con esta data!
Desde La Plata te mando un abrazo, y muchas gracias!
andrew, 12 Años Antes
Muchísima suerte con tu parcial, me alegro de que te sirvan los contenidos 🙂 Un saludo
QuimiTube, 12 Años Antes
te hago una consulta, esta teoria de bandas se que explica el brillo de los metales y la variacion de los puntos de fucion, pero no se como explicarlo con mis palabras…no me darias una mano???
Gracias!!
andrew, 12 Años Antes
Excelente explicacion. Comparto lo que dicen guille01 y Gustavo. Eres muy buena en esto… se nota. Saludos, y muy bien.
Manuel, 11 Años Antes
¡Muchas gracias!
QuimiTube, 11 Años Antes
Me gustaria saber quien o quienes redactaron lo que leí, o si es un autor corporativo (Quimitube, en este caso). Gracias 🙂
Manuel, 11 Años Antes
Hola Manuel:
La misma profesora que imparte las clases en los vídeos redacta todos los contenidos de la web.
Un saludo
QuimiTube, 11 Años Antes
Muchas gracias, le entiendo un poco más, el problema es que mi maestra no me enseño bandas de valencia con los nuemros cuanticos si no, nomas una pasada de este tema y en el examen valia 15 pts… :S pero espero pasar mi segunda oportunidad, gracias por esta pagina, y estas muy bonita :3 cuidate saludos
Arim, 11 Años Antes
Hola! muchas gracias por el video. Está fenomenal.
Hay una cosa que me cuesta entender..
Como sabes la variación de energia que hay entre la banda de valencia y la de conducción? te tendrían que dar los valores o te vale con hacer un diagrama de orbitales moleculares o sabiendo cuales son más o menos conductores? No entiendo muy bien como sabes cuando están más o menos separadas.
Muchas gracias y ¡Feliz año!
carmen, 11 Años Antes
Muchas gracias, me alegra que te sirva.
Efectivamente no puedes saberlo a priori, si te piden comparar te tendrán que dar los valores de energía de las distintas bandas o sus intervalos para que puedas evaluar cuál será más conductor o cuál menos; tal vez te digan cuál es el más conductor y cuál el menos y te hagan elegir entre una serie de valores, pero en todo caso tú no tienes que saber esos valores, siempre te los tendrán que aportar. Espero que te sirva la respuesta. Feliz año a ti también 🙂
QuimiTube, 11 Años Antes
En un elemento que tenga una banda de conducción totalmente llena de electrones, ¿sería un aislante?
Rubén, 11 Años Antes
Bueno, si tenemos un elemento con la banda de conducción ocupada no conduciría la corriente. Sin embargo, estrictamente hablando, un aislante es aquel elemento que tiene las dos bandas muy separadas y por tanto que es muy improbable que algún electrón alcance la banda de conducción.
QuimiTube, 11 Años Antes
Hola que tal
felicidades es muy buena explicación acerca de la teoría de las bandas…
pero solo tengo una duda como puedo saber que entre la banda de valencia y la banda de conducción existe ese espacio o salto energético
Erik Lopez, 11 Años Antes
Hola Erik, el hecho de que el material no conduzca la electricidad ya te está indicando que existe el salto, aunque no sé si te refieres a cómo determinarlo… Un saludo.
QuimiTube, 11 Años Antes
La mejor explicacion del tema que he visto, ojala fueras mi profesora, lo que explicaste en 12 minutos mi profesor lo hizo en 2 horas y aun asi ni el se entendia. Graciasssssssssssssss
julian, 11 Años Antes
¿Como se aplica la teoría de bandas si nos encontramos con un compuesto como por ejemplo el Cloruro Sódico (Na Cl)?
Victor, 10 Años Antes
Hola Víctor, en ese caso no sueles aplicarla porque no se trata de un metal sino de un compuesto iónico, el cual no conduce la electricidad en estado sólido (sí fundido). Aún así, si quieres esquematizar el hecho de que no sea conductor, podrías dibujar una banda de valencia y una banda de conducción muy alejadas entre sí.
QuimiTube, 10 Años Antes
es la primera vez que me entero de la teoria de bandas!!!!!! un milagro,estoy en 2 año de ingenieria mecanica y me has salvado la vida!deberia averte descubierto antes…muchas gracias!!!!
Marina, 10 Años Antes
¡Hola Marina! Me alegra mucho que te haya servido, lo intenté simplificar al máximo porque realmente la teoría de bandas es realmente compleja, pero es importante comprender la base. Un saludo grande y suerte con tus estudios.
QuimiTube, 10 Años Antes
¡Muchas gracias!
En diez minutos comprendí lo que no alcancé a entender en una clase de hora y media.
Dani, 10 Años Antes
Me alegra que te sirviera, muchas gracias por tu comentario y bienvenido.
QuimiTube, 10 Años Antes
No sé si tiene algo que ver la persona que lleva la página pero sinceramente estoy bastante harto de la cantidad de publicidad de takis y otros productos que me aparecen y se vuelve repetitiva en cada video, si la página cobra algo por esta publicidad que la reduzca porque hay usuarios que prefieren ver otras páginas aunque esta sea mejor a causa de la exasperación que produce esta publicidad masiva.
manolo, 10 Años Antes
Hola Manolo, lamento los inconvenientes, nosotros no regulamos la frecuencia publicitaria sino que lo hace una empresa externa (en teoría sí que podríamos regularla, si bien he estado comprobando que efectivamente hay algún error que hace que el parámetro se ignore y se muestre mucho más de lo estipulado). De momento lo hemos pausado, pero espero que comprendas que no podemos retirar la publicidad de la página de forma total ni definitiva (al menos de momento, sin otras fuentes alternativas) porque es la única y exigua fuente de ingresos que tenemos para pagar materiales, focos, cámara, servidor y otros gastos que necesitamos para mantener la página activa (y que no paga ni nuestro tiempo ni nuestro esfuerzo). Te pido que tengas también algo de paciencia y comprensión, dedicamos mucho a esta página. Un saludo.
QuimiTube, 10 Años Antes
[…] http://www.quimitube.com/videos/enlace-metalico-teoria-de-bandas […]
El salto de la conducción. | roles95, 10 Años Antes
Soy profesor de química de bachillerato y envidio la claridad y sencillez de su método. Gracias y felicitaciones por la yuda tan valiosa que presta a slos jóvenes estudiantes con sus clases virtuales. Desde Colombia, en Bucaramanga.
VICTOR MANUEL ACEVEDO PRADA, 9 Años Antes
Hola Víctor Manuel, muchísimas gracias, es un honor viniendo de un colega. Un saludo grande.
QuimiTube, 9 Años Antes
Muy bien explicado. Muchas gracias por la ayuda, me ha sido de gran utilidad para mi examen del martes. Ánimo
Oscar, 9 Años Antes
Me gusto mucho la explicación. Sabes organizarte bien dando el tema.La verdad que te felicito porque explicas excelente!!! =)
Paula, 9 Años Antes
¡Muchas gracias Paula!
QuimiTube, 8 Años Antes
Creo que quimitube me va a salvar el examen de química final de primero de carrera… gracias xD
Pablo, 9 Años Antes
De nada, espero que así fuera 🙂 Un saludo.
QuimiTube, 8 Años Antes
Muy buena explicación..te felicito
Manuel Gonzales, 9 Años Antes
¡Muchas gracias!
QuimiTube, 9 Años Antes
muchas mucgas gracias aprobe el final de quimica con una buena nota gracias a sus videos
gissel, 9 Años Antes
Me alegra mucho Gissel, enhorabuena!
QuimiTube, 9 Años Antes
¿por qué un aislante tiene las bandas de energía muy separadas y los conductores juntas o superpuestas?
¿Se observó empíricamente o se puede explicar teóricamente?
Joan, 9 Años Antes
Es una teoría, pero como tal explica plenamente todas las observaciones empíricas realizadas sobre conducción.
QuimiTube, 9 Años Antes
TE EXPLICAS DE MARAVILLA! OLE TÚ ^^
Vanessa M, 9 Años Antes
Muchas gracias!!
QuimiTube, 8 Años Antes
Hola que tal! Muchas felicidades por tu esfuerzo en la página, explicas muy bien. Me has ayudado varias veces. Saludos
Leonel B, 8 Años Antes
¡Hola! Me alegro mucho que te sirva, un saludo grande.
QuimiTube, 8 Años Antes
Sinceramente, la teoría de bandas no la veo muy útil para intentar para explicar en enlace metálico. Saludos
nico, 7 Años Antes