Reacción entre el yodo y el aluminio: ¡fuego!
Escrito por Quimitube el 10 enero
Hace unos días, en el canal de Youtube reaccionaexplota de la Cátedra de Cultura Científica y Comunicación Digital (Universitat de Girona) subieron un vídeo sobre la reacción entre el yodo y el aluminio.
En él se observa cómo inicialmente se pulveriza una mezcla de ambos reactivos sólidos, aluminio y yodo, en un mortero. ¿Por qué se hace esto? Porque, según veremos en el tema de cinética química, el grado de división de los reactivos afecta a la velocidad de reacción. Los reactivos pulverizados reaccionarán entre sí a mucha mayor velocidad que en grano grueso porque aumentará la superficie de contacto entre ellos y, por tanto, el número de colisiones eficaces que lleven a la obtención de productos. De hecho, como se ve en el vídeo, la reacción es rápida en cuanto se adicionan dos gotitas de agua. Empiezan desprendiéndose intensos vapores de yodo (yodo molecular, I2, ya que éste sublima fácilmente al empezar la reacción y aumentar la temperatura del medio) y posteriormente aparecen unas llamaradas, por tratarse de una reacción fuertemente exotérmica. Se está formando el compuesto yoduro de aluminio, AlI3, es decir:
Por tanto, se trata de una reacción de oxidación reducción, ya que hay cambios en los estados de oxidación de ambos reactivos. El yodo se reduce, pasando de un estado de oxidación 0 a un estado de oxidación -1, y el aluminio se oxida, pasando de un estado de oxidación 0 a un estado de oxidación +3.
Como vemos, con esta reacción sencilla podemos hablar de varios temas distintos de los que se tratan en segundo de bachillerato: cinética química, termoquímica y redox. Es más, la reacción también nos permite hablar de enlace químico y de geometría molecular, ya que el yoduro de aluminio puede formar un dímero Al2I6 de estructura muy particular:
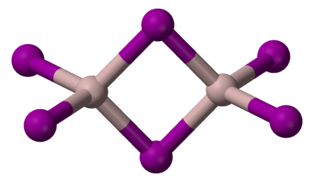
Por lo que la reacción podríamos escribirla del siguiente modo:
Una prueba de que la química es una sola y de que es importante comprender que el estudio de una misma reacción química, o de un compuesto, se puede llevar a cabo desde distintas perspectivas, pero sin cambios sustanciales y sin compartimentar tanto como acostumbramos.





[…] Reacción química redox exotérmica entre el yodo molecular y el aluminio metálico para dar un dímero de yoduro de aluminio, Al2I6. […]
Reacción química entre el yodo y ..., 12 Años Antes
Se puede utilizar yodo pero liquido? o donde consigo en polvo ayuda!!!!!!!!!!!
Cinthya, 11 Años Antes
¡Hola! Lo siento, yo no he probado la reacción personalmente, pero dudo que te vaya bien con el líquido… O tal vez pueda ser peligroso.
QuimiTube, 11 Años Antes